Victor Rubio Rojas
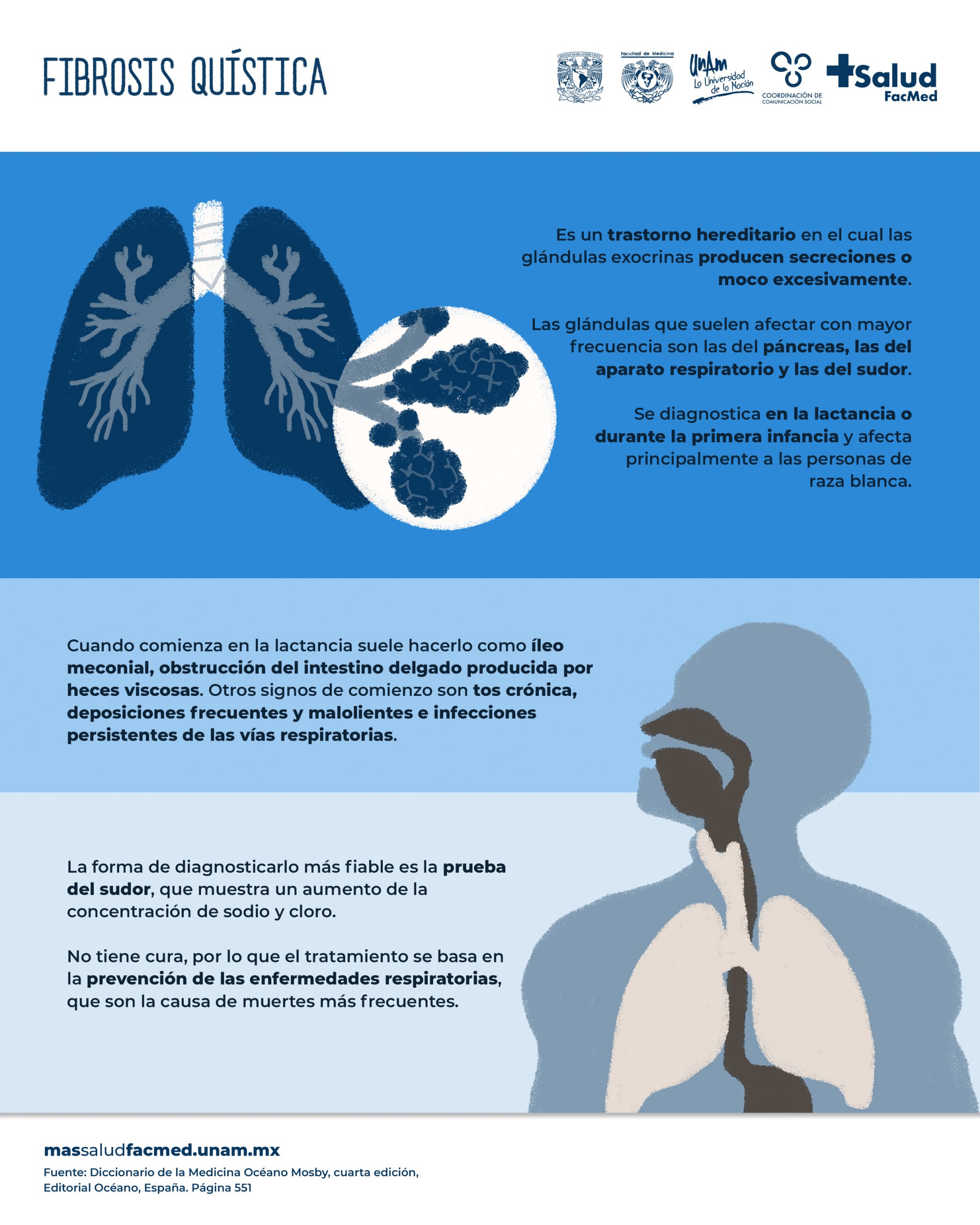
Se trata de una enfermedad genética que produce disfunción de las glándulas exócrinas. Éstas son glándulas que secretan productos químicos a través de conductos o tubos y llevan las secreciones producidas a una cavidad corporal, a la luz de un órgano o a la superficie corporal.
Esta disfunción glandular conduce a diversas alteraciones gastrointestinales y en las vías aéreas produce obstrucción crónica e infección. Constituye la causa más frecuente de enfermedad pulmonar grave en la infancia, además de presentarse con poliposis nasal, pansinusitis, prolapso rectal, colelitiasis e hiperglucemia insulinodependiente.
El cuadro clínico respiratorio es producido por la falta de aclaramiento de las bacterias inhaladas lo que produce inflamación y sobreinfección por múltiples gérmenes como S. aureus, B. cepaceae, Burkholderia y P. aeruginosa.
Existen algunas características típicas que pueden reconocerse según la edad del paciente; así, en los recién nacidos y hasta al mes de edad, se observa bloqueo del intestino delgado causado por meconio, también llamado íleo meconial y coloración amarilla de la piel y mucosas o ictericia prolongada.
Hasta los dos años con presencia de secreciones lipídicas en las heces o esteatorrea, retraso del crecimiento, deshidratación con alteraciones electrolíticas e infecciones respiratorias de repetición.
De los dos a los doce años con infecciones respiratorias de repetición, pólipos y dilataciones bronquiales, también llamadas bronquiectásias, donde se acumula gran cantidad de secreciones.
Después de los doce años con insufiencia respiratoria, bronquiectasias, esterilidad, diabetes mellitus asociada a fibrosis quistica, afectación hepática y litiasis biliar.
Aunque existen diversos estudios para valorar la función de cada órgano afectado, los criterios diagnósticos para esta enfermedad incluyen una prueba del sudor positiva, confirmación con estudios de DNA y una o más de las siguientes enfermedades: enfermedad pulmonar crónica, insuficiencia pancreática exócrina, antecedentes familiares positivos y tamiz neonatal positivo.
El tratamiento va encaminado a controlar las manifestaciones clínicas en los distintos aparatos, además de un régimen nutricional especializado, así como a la prevención, control y tratamiento de las complicaciones respiratorias y digestivas.
Cabe destacar que, si se inicia el tratamiento antes de que la función pulmonar esté severamente deteriorada, cerca del 90% de los pacientes sobreviven después de los 20 años. La causa más frecuente de muerte se debe a la afectación respiratoria.
Referencias:
1.- Isabel Largo García (2009). «Fibrosis quística». Revista Pediatría Electrónica 6. ISSN 0718-0918. Archivado desde el original el 3 de marzo de 2016
2.- Rowe SM, Miller S, Sorscher EJ. «Cystic Fibrosis.» N Engl J Med. 2005 may 12;352(19):1992-2001.
3.- Eggermont E, De Boeck K. «Small-intestinal abnormalities in cystic fibrosis patients.» Eur J Pediatr. 1991 oct;150(12):824-8. Rev.
4.- Cohn JA, Friedman KJ, Noone PG, Knowles MR, Silverman LM, Jowell PS. Relation between mutations of the cystic fibrosis gene and idiopathic pancreatitis. N Engl J Med. 1998 sep 3;339(10):653-8.
5.- Stern, RC. «The diagnosis of cystic fibrosis.» N Engl J Med 1997; 336:487.
6.- Ramalho AS, Beck S, Meyer M, Penque D, Cutting GR, Amaral MD. Five percent of normal cystic fibrosis transmembrane conductance regulator mRNA ameliorates the severity of pulmonary disease in cystic fibrosis. Am J Respir Cell Mol Biol. 2002 nov;27(5):619-27.
7.- Cystic Fibrosis Foundation data (PDF) Archivado el 24 de julio de 2006 en la Wayback Machine.